沈伟教授课题组在《PLOS BIOLOGY》发表论文解析原始卵泡形成机制
近日,青岛农业大学生命科学学院、生殖科学研究院沈伟教授课题组在自然指数期刊、一区TOP期刊《PLOS BIOLOGY》上发表有关卵巢原始卵泡组装的遗传调节机制的研究论文。该文第一作者为博士生王俊杰,通讯作者为沈伟教授,青岛农业大学为第一单位。该研究得到国家重点研发计划、国家自然科学基金和山东省泰山学者工程等项目资助。
目前,面对日益增长的生活和工作压力、环境改变以及外源有害物质影响,生殖健康问题困扰着越来越多的生育适龄女性。生殖生物学家普遍认为,人和哺乳动物的原始卵泡库一旦形成,在数量上便不再增加,青春期后会随排卵周期而不断减少直至耗竭。因此,以原始卵泡(由一个卵母细胞和周围包裹的单层扁平颗粒细胞组成的结构)为主的有限卵巢储备对人和哺乳动物的生育期限显得尤其重要。人和动物的原始卵泡形成过程涉及颗粒细胞的分化和增殖、雌性生殖细胞第一次减数分裂前期双线期阻滞、生殖细胞簇解聚、生殖细胞的大量丢失、原始卵泡组装等多个生物学事件,同时需要卵巢中多种细胞的共同参与和协同调控。因此,繁多的生物学事件和复杂的多细胞调控网络使得对原始卵泡形成机制的遗传解析举步维艰。
针对原始卵泡形成过程的细胞异质性问题,沈伟课题组以单细胞分辨率解析原始卵泡形成的分子调控机制。该研究选取原始卵泡形成前、中、后三个关键发育节点进行单细胞基因表达模式分析,成功鉴定出雌性生殖细胞和颗粒细胞发育阶段特异性标记基因,解析了原始卵泡组装相关生物学事件的关键调节机制。该研究发现,M1ap编码第一次减数分裂前期阻滞所需的关键蛋白,Hspb11通过维持线粒体膜稳定调控细胞凋亡;Eif4a1和G3bp2调节卵泡形成过程相关的mRNA转录活动;Ooep基因编码一种母系蛋白复合物成分并参与同源重组,在原始卵泡组装的后期才开始表达。该研究进一步构建了卵巢细胞的单细胞发育轨迹,将原始卵泡组装过程的雌性生殖细胞划分为三个发育阶段,通过功能分析揭示FoxO和Hippo信号通路以及组蛋白修饰可能是影响原始卵泡形成的重要途径之一。另外,筛选得到雌性生殖细胞在原始卵泡组装时期的转录因子,其中Nr3c1、Foxo1、Brca1、Kdm5a和Kdm5b等转录因子集中体现在卵泡形成前的生殖细胞簇,Smarcb1、Hes1、Stat3和Sox1等仅在形成的卵泡中特异性高表达,并在原始卵泡形成过程中发挥重要的调控作用。该研究为系统揭示原始卵泡形成的分子机制提供了重要参考。
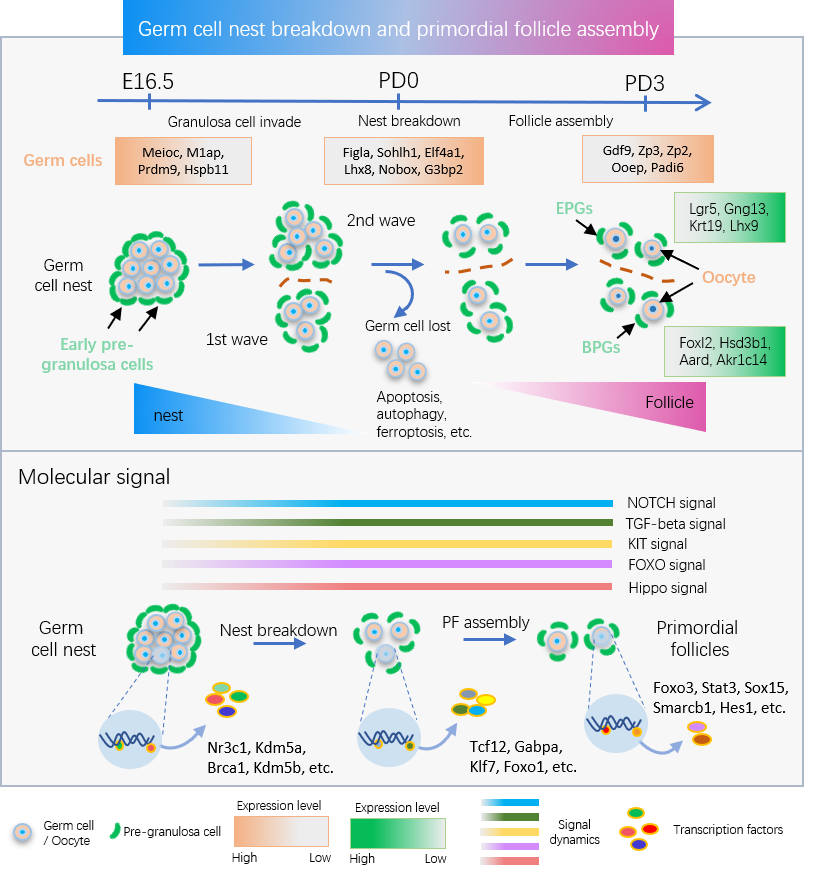
图为原始卵泡形成过程的基因表达动态变化和分子调控网络
原文链接:Single-cell transcriptome landscape of ovarian cells during primordial follicle assembly in mice. PLoS Biol, 2020, 18(12): e3001025. https://doi.org/10.1371/journal.pbio.3001025
- 上一篇: 没有了
- 下一篇: 没有了
地址:山东省 青岛市 城阳区 长城路700号
邮编:266109
电话:0532-58957473
邮箱:xwzx@qau.edu.cn














.jpg)
.png)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)


